Câu 2: Cân bằng các phản ứng sau và phân loại phản ứng hóa hợp và phản ứng phân hủy?
A. Fe(OH)3 → Fe2O3 + H2O
B. CaO + CO2 → CaCO3
C. Al + O2 → Al2O3
D. KClO3 → KCl + O2
Lập PTHH của phản ứng và cho biết phản ứng nào là phản ứng hóa hợp, phân hủy và thế.
1.H2SO4+AL(OH)3--->AL2(SO4)3+H2O
2.Ba(NO3)2+Na2SO4---->BaSO4+NaNO3
3.KClO3---->KCl+02
4.NaHS+KOH---->Na2S+K2S+H2O
5.Fe(OH)2+O2+H20---->HNO3
6.NO2+O2+H2O---->HNO3
1. \(3H_2SO_4+2Al\left(OH\right)_3\rightarrow Al_2\left(SO_4\right)_3+6H_2O\) - Pư thế
2. \(Ba\left(NO_3\right)_2+Na_2SO_4\rightarrow BaSO_4+2NaNO_3\) - Pư thế
3. \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\) - Pư phân hủy.
4. \(2NaHS+2KOH\rightarrow Na_2S+K_2S+2H_2O\) - Pư thế
5. \(4Fe\left(OH\right)_2+O_2+2H_2O\rightarrow4Fe\left(OH\right)_3\) - Pư hóa hợp.
6. \(4NO_2+O_2+2H_2O\rightarrow4HNO_3\) - Pư hóa hợp.
pư thế
pư thế
pư phân hủy
pư phân hủy
pư hóa hợp
pư hóa hợp
![]()
Hãy lập các phương trình hóa học sau đây và cho biết phản ứng thuộc loại phản ứng hóa hợp hay phản ứng phân hủy?
a) KMnO4 à K2MnO4 + MnO2 + O2
b) Fe + O2 à Fe3O4
c) P + O2 à P2O5
d) HgO à Hg + O2
e) KClO3 à KCl + O2
f) Mg + O2 à MgO
g) Fe(OH)3 à Fe2O3 + H2O
h) N2 + O2 à N2O5
Phản ứng phân hủy : a ; d ; e ; g
Phản ứng hóa hợp : b ; c ; f ; h
\(a) 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ b) 3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\\ c) 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\\ d) 2HgO \xrightarrow{t^o} 2Hg + O_2\\ e) 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ f) 2Mg + O_2 \xrightarrow{t^o} 2MgO\\ g) 2Fe(OH)_3 \xrightarrow{t^o} Fe_2O_3 + 3H_2O\\ h) 2N_2 + 5O_2 \xrightarrow{t^o,xt} 2N_2O_5\)
\(a.2KMnO_4\underrightarrow{^{t^0}}K_2MnO_4+MnO_2+O_2\left(PH\right)\)
\(b.3Fe+2O_2\underrightarrow{^{t^0}}Fe_3O_4\left(HH\right)\)
\(c.4P+5O_2\underrightarrow{^{t^0}}2P_2O_5\left(HH\right)\)
\(d.2HgO\underrightarrow{^{t^0}}2Hg+O_2\left(PH\right)\)
\(e.2KClO_3\underrightarrow{^{t^0}}2KCl+3O_2\left(PH\right)\)
\(f.2Mg+O_2\underrightarrow{^{t^0}}2MgO\left(HH\right)\)
\(g.2Fe\left(OH\right)_3\underrightarrow{^{t^0}}Fe_2O_3+3H_2O\left(PH\right)\)
\(h.N_2+\dfrac{5}{2}O_2\underrightarrow{^{t^0}}N_2O_5\left(HH\right)\)
Lập PTHH của phản ứng và cho biết phản ứng nào là phản ứng hóa hợp, phân hủy và thế.
7.SO2+Br2+H20---->H2SO4+HBr
8.Fe3O4+HCl---->FeCl2+FeCL3+H20
9.FeS+O2---->Fe2O3+SO2
10.Fe3O4+Al----->Fe+Al2O3
11.Fe(OH)3----->Fe2O3+H20
12.KMnO4+HCl---->Cl2+KCl+MnCI2+H20
13.Zn+2HCI----->ZnCL2+H2
7.SO2+Br2+2H20->H2SO4+2HBr(phản ứng thế)
8.Fe3O4+8HCl->FeCl2+2FeCL3+4H20(phản phân huỷ)
9.4FeS+7O2->2Fe2O3+4SO2 (phản ứng thế)
10.3Fe3O4+8Al->9Fe+4Al2O3 (phản ứng thế)
11.2Fe(OH)3->Fe2O3+3H20(phản ứng phân huỷ)
12.2KMnO4+16HCl->5Cl2+2KCl+2MnCI2+8H20(phản ứng phân huỷ)
13.Zn+2HCI->ZnCL2+H2(phản ứng thế)
Cân bằng các phương trình phản ứng oxi hóa – khử sau đây bằng phương pháp thăng bằng electron và cho biết chất khử, chất oxi hóa ở mỗi phản ứng:
a) Al + Fe3O4 → Al2O3 + Fe
b) FeSO4 + KMnO4 + H2SO4 → Fe2(SO4)3 + MnSO4 + K2SO4 + H2O
c) FeS2 + O2 → Fe2O3 + SO3
d) KClO3 → KCl + O2
e) Cl2 +KOH → KCl + KClO3 + H2O
Cân bằng các phương trình phản ứng oxi hóa – khử:
![]()
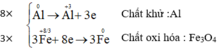
![]()
![]()

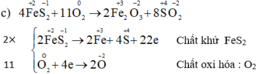

Câu 2: Phản ứng nào dưới đây không phải là phản ứng phân hủy?
A. 2 KMnO4 → K2MnO4 + MnO2 + O2 C. CuO + H2 -> Cu + H2O
B. 2Fe(OH)3 → Fe2O3 + 3H2O D. CaCO3 → CaO + CO2
Câu 2: Phản ứng nào dưới đây không phải là phản ứng phân hủy?
A. 2 KMnO4 → K2MnO4 + MnO2 + O2 C. CuO + H2 -> Cu + H2O
B. 2Fe(OH)3 → Fe2O3 + 3H2O D. CaCO3 → CaO + CO2
Bài 2: Cân bằng các phản ứng hóa học sau và xác định xem chúng thuộc loại phản ứng nào?
a/ KNO3 → KNO2 + O2↑
b/ Al(OH)3 → Al2O3 + H2O
c/ Ag + Cl2 → AgCl
d/ KClO3→ KCl + O2↑
e/ Mg + HCl → MgCl2 + H2
f/ P2O5+ H2O → H3PO4
g/ KMnO4 → K2MnO4 + MnO2 + O2
h/ Fe + CuCl2 → FeCl2 + Cu
i/ Fe3O4 + H2 → Fe + H2O
j/ Al + O2 → Al2O3
2KNO3 -> (t°) 2KNO2 + O2 (phản ứng phân hủy)
2Al(OH)3 -> Al2O3 + 3H2O (phản ứng phân hủy)
2Ag + Cl2 -> (ánh sáng) 2AgCl (phản ứng hóa hợp)
2KClO3 -> (t°, MnO2) 2KCl + 3O2 (phản ứng phân hủy)
Mg + 2HCl -> MgCl2 + H2 (phản ứng thế)
P2O5 + 3H2O -> 2H3PO4 (phản ứng hóa hợp)
2KMnO4 -> (t°) K2MnO4 + MnO2 + O2 (phản ứng phân hủy)
Fe + CuCl2 -> FeCl2 + Cu (phản ứng thế)
Fe3O4 + 4H2 -> (t°) 3Fe + 4H2O (phản ứng oxi hóa khử)
4Al + 3O2 -> (t°) 2Al2O3 (phản ứng hóa hợp)
a/ 2KNO3 → 2KNO2 + 3O2↑
b/ 2Al(OH)3 → Al2O3 + 3H2O
c/ 2Ag + Cl2 → 2AgCl
d/ 2KClO3→ 2KCl + 2O2↑
e/ Mg + 2HCl → MgCl2 + H2
f/ P2O5+ 3H2O → 2H3PO4
g/ 3KMnO4 → K2MnO4 + MnO2 + O2
h/ Fe + CuCl2 → FeCl2 + Cu
i/ Fe3O4 + 4H2 → 3Fe + 4H2O
j/ 4Al + 3O2 → 2Al2O3
a/ 2KNO3 → 2KNO2 + O2↑ : pứ phân hủy
b/ 2Al(OH)3 → Al2O3 + 3H2O : pứ phân hủy
c/ 2Ag + Cl2 →2 AgCl : pứ hóa hợp
d/ 2KClO3→ 2KCl + 3O2↑ : pứ phân hủy
e/ Mg + 2HCl → MgCl2 + H2 : pứ thế
f/ P2O5+ 3H2O → 2H3PO4 : pứ hóa hợp
g/ 2KMnO4 → K2MnO4 + MnO2 + O2 : pứ phân hủy
h/ Fe + CuCl2 → FeCl2 + Cu : pứ thế
i/ Fe3O4 + 4H2 → 3Fe + 4H2O : pứ oxi hóa-khử
j/4 Al + 4O2 → 2 Al2O3 : pứ hóa hợp
Cân bằng phương trình hoá học của các phản ứng và cho biết trong các phản ứng sau nào thuộc loại phản ứng hóa hợp? Phản ứng nào thuộc loại phản ứng phân hủy?
1. H2SO4+ Al(OH)3- - -> Al2(SO4)3 + H2O
2. Ba(NO3)2+ Na2SO4- - -> BaSO4 + NaNO3
3. KClO3 ----> KCl + O2
4. NaHS + KOH ------> Na2S + K2S + H2O
5. Fe(OH)2+ O2 + H2O ------> Fe(OH)3
6. NO2 + O2 + H2O ------> HNO3
7. SO2 + Br2 + H2O ------> H2SO4 + HBr
8. Fe3O4 + HCl -----> FeCl2 + FeCl3 + H2O
9. FeS + O2 -----> Fe2O3 + SO2
10. Fe 3O4+ Al -------> Fe + Al2O3
11. Fe(OH)3-----> Fe2O3 + H2O
12. KMnO4+ HCl -----> Cl2 + KCl + MnCl2 + H2O
1) 2Al(OH)3 + 3H2SO4 --> Al2(SO4)3 + 6H2O
2) Ba(NO3)2 + Na2SO4 --> BaSO4 + 2NaNO3
3) 2KClO3 --to--> 2KCl + 3O2
4) 2NaHS + 2KOH --> Na2S + K2S + 2H2O
5) 4Fe(OH)2 + O2 + 2H2O --> 4Fe(OH)3
6) 4NO2 + O2 + 2H2O --> 4HNO3
7) SO2 + Br2 + 2H2O --> H2SO4 + 2HBr
8) Fe3O4 + 8HCl --> FeCl2 + 2FeCl3 + 4H2O
9) 4FeS + 7O2 -to--> 2Fe2O3 + 4SO2
10) 3Fe3O4 + 8Al --to--> 9Fe + 4Al2O3
11) 2Fe(OH)3 --to--> Fe2O3 + 3H2O
12) 2KMnO4 + 16HCl --> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
Pư hóa hợp: 5,6
Pư phân hủy: 3,11
1. 3H2SO4+ 2Al(OH)3 → Al2(SO4)3+ 6H2O (phản ứng thế)
2. Ba(NO3)2 + Na2SO4 → BaSO4 + 2NaNO3 (phản ứng thế)
3. 2KClO3 → 2KCl + 3O2 (phản ứng phân hủy)
4. 2NaHS + 2KOH → Na2S + K2S + 2H2O (phản ứng thế)
5. 4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3 (phản ứng hóa hợp)
Cân bằng các phương trình phản ưng sau và cho biết trong các phản ứng này, phản ứng nào là phản ứng hóa hợp, phản ứng nào là phản ứng phân hủy?
a) Mg + O2 --> MgO | f) Fe + HCl ---> FeCl2 + H2 |
b) H2 + O2 --> H2O | g) Na2O + H2O ---> NaOH |
c) P + O2 --> P2O5 | h) Fe2O3 + H2 ---> Fe + H2O |
d) KMnO4 --------> K2MnO4 + MnO2 + O2 | i) CH4 + O2 ---> CO2 + H2O |
e) KClO3 ------> KCl + O2 | k) CxHyO + O2 ---> CO2 + H2O |
giúp với ạ:,00
a. Mg + O2 -> 2MgO ( Phản ứng hóa hợp )
b. 2H2 + O2 -> 2H2O ( Phản ứng hóa hợp )
c. 4P + 5O2 -> 2P2O5 ( Phản ứng hóa hợp )
d. 2KMnO4 -> K2MnO4 + MnO2 + O2 ( Phản ứng phân hủy )
e. 2KClO3 -> 2KCl + 3O2 ( Phản ứng phân hủy )
f. Fe + 2HCl -> FeCl2 + H2 ( Phản ứng thế)
g. Na2O + H2O -> 2NaOH ( Phản ứng hóa hợp )
h. Fe2O3 + 3H2 -> 2Fe + 3H2O ( Phản ứng thế )
i. CH4 + 2O2 -> CO2 + 2H2O ( Phản ứng thế )
5. KClO3 bị nhiệt phân hủy theo phương trình phản ứng KClO3 → KCl + O2 Em hãy cân bằng phương trình phản ứng trên và tính thể tích O2 (đktc) thu được khi phân hủy 49 gam KClO3
\(n_{KClO_3}=\dfrac{m}{M}=\dfrac{49}{39+35,5+16\cdot3}=0,4\left(mol\right)\)
\(PTHH:2KClO_3-^{t^o}>2KCl+3O_2\)
tỉ lệ 2 : 2 : 3
n(mol) 0,4----------->0,4--->0,6
\(V_{O_2\left(dktc\right)}=n\cdot22,4=0,6\cdot22,4=13,44\left(l\right)\)